- По періодах неметалічні властивості: дослідження впливу та особливостей
- Періодична система хімічних елементів
- Загальні характеристика періодів
- Зміни неметалічних властивостей від періоду до періоду
- Період перший: винятки та іонізація
- Другий період: баланс сили та грації
- Третій період: неметал у кожній комірчині
- Четвертий період: більше елементів, більше можливостей
- П’ятий та шостий періоди: коли стають видимими межі
- Вплив з’єднань та реакцій
- Таблиця: Неметалічні властивості по періодах
По періодах неметалічні властивості: дослідження впливу та особливостей
По періодах неметалічні властивості елементів стають ключовою темою, коли йдеться про їх хімічну поведінку. Тут ми детально розглянемо, які фактори впливають на неметалічність елементів, і як ці особливості змінюються по періодичній системі.
Періодична система хімічних елементів
Отже, що таке періодична система хімічних елементів? Це наче таблиця-гігант, де всі елементи впорядковані на основі їх атомних номерів. Ви лише уявіть, що кожен період демонструє зміни в неметалічних властивостях. І це вражає!
Загальні характеристика періодів
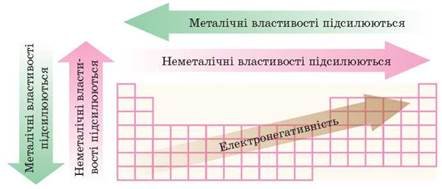
- Періоди показують поступове наростання енергії іонізації.
- Чітко просліджується зменшення металевих властивостей.
- Неметалічні властивості проявляються яскравіше наприкінці кожного періоду.
Зміни неметалічних властивостей від періоду до періоду
Соло для неметалічних властивостей, сер! Тут кожен період, наче симфонія змін. Чим далі, тим більше неметалічності утворилися у властивостях елементів. Поїхали!
Період перший: винятки та іонізація
Перший період, він же наче фортепіанний вступ. Не тільки малий за розміром, але й відносно простий. В ньому лише два елементи — водень та гелій. І ось у чому прикол:
- Водень – типова неметал, малий, але мегаважливий.
- Гелій – інертний газ, але теж з мінімальними металевими ознаками.
Якщо глянути на ці два елементи під мікроскопом, ви побачите: неметалічні властивості переважають. Це як два віддані неметалічні хлопці, які не мають куди податись.
Другий період: баланс сили та грації
Ось вони — славнозвісні карбону, азоту, кисню. Вони ніби балерини на просторах хімії, делікатно проявляючи свої неметалічні властивості. Ось кілька фактів:
- Багато неметалічних елементів, зокрема, кисень та азот.
- Сильна електронегативність. О, ця суцільно затягуюча силичка…
- Ковалентні зв’язки між атомами — справжня знахідка для хіміка.
На кінець цього періоду вже точно знаєш: неметалічні властивості — це сила, яка важлива.
Третій період: неметал у кожній комірчині
Третій період стає багатшим на неметали, і ми їх знаємо краще. Фосфор, сірка, хлор — всі вони несуть неметалічне слово в цей світ. І давайте їх трохи розливаємо на столі:
- Зростання електронегативності: цей показник зростає справа наліво.
- Майже кожен елемент у кінці періоду — неметал!
- Оксиди елементів проявляють кислотне середовище. Незначно, але помітно.
І так, це місце розквіту неметалічних властивостей.
Четвертий період: більше елементів, більше можливостей
Четвертий період. Він як великий магазин на розі: багатий і розмаїтий. Тут з’являються новачки-наметали, які долають тяжіння металу:
- Збільшення електронегативності й складності властивостей.
- Помітніша різниця між металами та неметалами.
- Постійні сплески оксидних властивостей.
І ось ви вже самі відчуваєте, як ці зміни наростають і які перспективи несуть для нас, хіміків.
П’ятий та шостий періоди: коли стають видимими межі
До п’ятого та шостого періодів ми прибуваємо на епіцентр змін. Це як куліси з нових можливостей, і рух повільний, але вірний:
- З’являються унікальні елементи, як йод та ксенон.
- Зростає роль кислотно-основних реакцій.
- Тут вже неметали дихають на повні грудь.
І саме тут, у роцістрічних моментів, розквіту досягається особливий рівень неметалічних властивостей. Ви наче дивитесь на новий вимір.
Вплив з’єднань та реакцій
Звісно, неметалічні властивості в періодах значно підсилюються за рахунок з’єднань і реакцій, які вони утворюють. Тут вже ми можемо оцінити всю хімічну силу, закладену в цих елементах:
- Ковалентні з’єднання домінують і роблять свою справу.
- Оксид сирцевих неметалів створюють нові форми речовин.
- Панівна електронегативність впливає на кислотно-основну поведінку.
Таблиця: Неметалічні властивості по періодах
| Період | Неметалічні Властивості |
|---|---|
| 1 | Водень, Гелій: проявляють слабкі неметалічні характеристики. |
| 2 | Карбон, Азот, Кисень: добре розвинута неметалічність, висока електронегативність. |
| 3 | Фосфор, Сірка, Хлор: сильні неметалічні властивості, зростання кислотності оксидів. |
| 4 | Завершення періоду: більш ясно виражені неметалічні властивості. |
| 5 і 6 | Йод, Ксенон: яскраві і насичені неметалічні властивості. |
Отже, неметалічні властивості по періодах — це не просто термін. Це цілий світ змін, де кожен період показує щось унікальне. Від першого до шостого, кожен має свою родзинку. Незважаючи на те, що життя швидкоплинне, ці зміни в хімії залишаються постійними. Ось так і живемо – спостерігаємо, досліджуємо, вивчаємо.







